
检测结肠直肠癌的血液检测即将获得 FDA 批准
【《华人》传媒编辑王惠豫 2024年5月26日】生产结肠直肠癌的血液检产品Shield的公司Guardant Health正在寻求美国食品及药物管理局(FDA)的上市前批准,以便对45岁及以上的平均风险人群进行结直肠癌筛查。
上周四,在 FDA 顾问小组会议上,8 位 FDA 独立顾问对安全性投了赞成票,1 位投了反对票。在疗效方面,六人投了赞成票,三人投了反对票。在效益大于风险方面,7 票赞成,2 票反对。

Shield 如何工作?
Shield 通过检测血液样本中肿瘤脱落的 DNA 来检测结直肠癌。实验室在收到样本后两周左右就会得出结果。
发表在《新英格兰医学杂志》上的临床试验数据显示,Shield 的灵敏度为 83.1%,这意味着 91% 通过结肠镜检查发现患有结直肠癌的患者在 Shield 血液检测中呈阳性。它的特异性也达到了 89.9%,即 89.9% 的无癌症患者在血液检测中呈阴性。
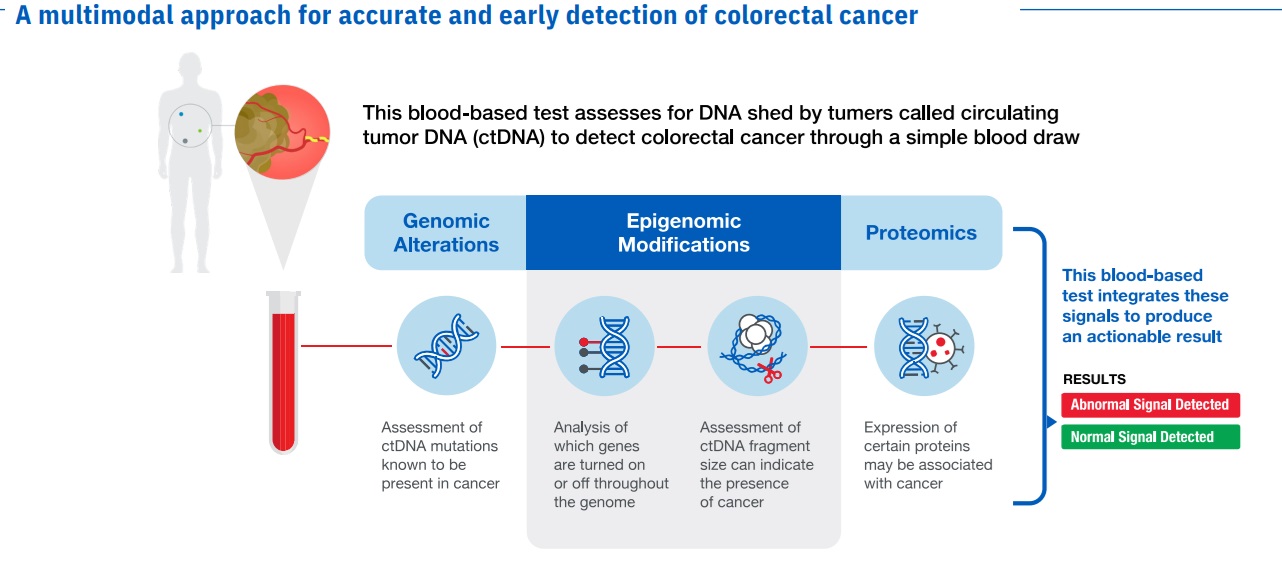
Guardant Health公司称,血液检测将有助于消除与当前筛查方法有关的障碍,如结肠镜检查或粪便检测,这些方法可能耗时或难以完成。该公司称,血液检测无需任何特殊准备,只需在医生的标准诊疗过程中进行即可。
Guardant Shield 血液检测已推出两年,费用为 900 美元。如果 Shield 获得 FDA 的全面批准,这将是第一个获得批准的符合医疗保险报销要求的结直肠癌血液筛查测试。
我医生鼓励年龄在 45 岁或以上、具有平均患病风险的人使用 Shield。 不建议那些被认为是个人或家族疾病史高风险的人。
虽然癌症死亡人数总体上有所下降,但美国癌症协会今年早些时候的一份报告发现,年轻成年人患结肠癌的人数增加令人担忧。目前,结肠癌是 50 岁以下男性的第一大死因,也是同一年龄组女性的第二大死因。
(来源:News 12 the Bronx, ABC)
# # # # #
本网站已经开通免费订阅功能,请在网页右上角输入您的电邮地址及名字(任何昵称)。订阅后您可以及时收到网站的更新通知。希望新老读者踊跃订阅,让我们有机会能够为您提供更好的服务。
请点击: 主页 ( https://wechineseus.com ) 浏览本网站更多的新闻和内容
请关注本网站在X (推特)的账户: https://twitter.com/wechineseinus












Comments powered by CComment